| 上传:邓菘化学 | 审核发布:admin | 更新时间:2016-1-13 15:00:50 | 点击次数:443次 |
“金属活动性顺序及其应用”
【考点1 】 考查金属活动性顺序的内容
★知识链接: K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、
Ag、Pt、Au,由金属活动性顺序的内容可知:活动性最强的金属是K,活动性最弱的金属是Au,能跟酸发生置换反应的金属的化学活动性比氢(H)强,能把另一金属从其可溶性盐溶液中置换出来的金属的活动性比盐中金属的活动性强。
1.下列金属的活动性顺序由强到弱排列正确的是
A.Mg>Fe>Cu B. Cu>Al>Ag C. Zn>Ag>Cu D .Cu>Fe>Mg
2.根据金属活动性顺序规律,可以判断出下列反应能进行的是 ( )
A.铜与盐酸 B.银与硫酸铜溶液 C.铁与硫酸锌溶液 D.铝与稀硫酸
3.已知X、Y、Z三种金属,它们在溶液中能发生如下反应: X + YCl2 → XCl2 + Y, Z + XCl2 → ZCl2 + X, X + HCl → XCl2 + H2↑ 则三种金属活动性顺序表里的位置可能是
A.Z、X、Y、(H) B.Y、(H)、X、Z C.X、Y、(H)、Z D.Z、X、(H)、Y
4.要验证镁、铁、铜三种金属活动顺序, 仅用组内物质可直接进行实验验证的是
A.Cu、FeCl2溶液、MgCl2溶液 B.Fe、Cu、MgCl2溶液
C.Mg、FeSO4溶液、CuCl2溶液 D.Fe、CuSO4溶液、MgCl2溶液
5.某学生为了验证铁、锌、铜三种金属的活动性顺序,设计了四种方案:①将Zn、Cu分别加入到FeSO4溶液中;②将Zn、Cu分别加入到ZnSO4溶液中;③将Zn分别加入到FeSO4、CuSO4溶液中;④将Fe 分别加入到ZnSO4、CuSO4溶液中。其中可行的是( )
A.①④ B.①② C.②③ D.③④
【考点2】考查金属与酸之间的置换反应
★知识链接:金属与酸发生置换反应产生氢气应具备的条件是:(1)金属的位置:在金属活动性顺序中,金属的位置要在氢(H)的前面;(2)酸要用无氧化性的酸,如盐酸、稀硫酸等;(3)硝酸具有氧化性与金属反应时一般生成水而不生成氢气,因而不发生置换反应。
6.下列金属跟酸能反应而放出氢气的是
A Fe和H2SO4 B Ag和稀HCl C Zn和HNO3 D Al和浓H2SO4
7.不能由金属直接与盐酸反应制得的是( )
A、MgCl2、 B、FeCl3、 C、AlCl3 D、CuCl2
8.现有甲、乙、丙、丁四种金属,将这四种金属粉末分别投人相同浓度的盐酸中,只有丙、丁发生反应并产生气泡,而且丁产生气泡比丙的更![]() 快;将甲投入
快;将甲投入![]() 乙的硝酸盐溶液中,有金属乙析出。这四种金属的活动性顺序是
乙的硝酸盐溶液中,有金属乙析出。这四种金属的活动性顺序是
A.丁>丙>甲>乙 B.乙>甲>丙>丁 C.丙>丁>甲>乙 D.丁>丙>乙>甲
【考点3 】考查对金属活动性强弱的判断
★知识链接:能跟酸发生置换反应的金属的化学活动性比氢(H)强;能把另一金属从其可溶性盐溶液中置换出来的金属的活动性比盐中金属的活动性强。
9.有X、Y、Z三种金属,将X、Y、Z分别浸入稀硫酸中,Z溶解,X和Y不溶解;将X浸入Y的硫酸盐溶液中,在X的表面由Y析出。则X、Y、Z的金属活动性由强到弱的顺序为
A.Z、Y、X B.Y、Z、X C.Z、X、Y D.Y、X、Z
10.现有X、Y、Z三种金属,只有X能与稀硫酸反应产生氢气,Y、Z则不能,但有下列反应关系:![]() ,则X、Y、Z三种金属的活动性顺序由强到弱的是
,则X、Y、Z三种金属的活动性顺序由强到弱的是
A.Z>Y>X B.X>Z>Y C.X>Y>Z D.Z>X>Y
11.金属X、Y、Z分别是Fe、Al、Cu、Ag中的一种。其中X能与稀H2SO4反应生成X2(SO4)3,而Y、Z不能与稀H2SO4反应;Y能与AgNO3溶液反应,而Z不能与AgNO3溶液反应。则X、Y、Z依次为( )A. Fe、Ag、Cu B. Fe、Cu、Ag C. Al、Cu、Ag D. Al、Ag、Cu
12.废旧手机的某些部件中含有Mg、Al、Cu、Ag等金属,为了回收重金属,将旧手机的部件粉碎并浸入足量稀硫酸中充分反应过滤,所得固体中含有的金属是:
A.Mg、Al B.Cu、Ag C.Al、Cu D.Mg、Ag
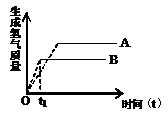 13.X、Y、Z三种金属的活动性,可用下列化学方程式说明:Z+Y(NO3)2===Z(NO3)2+Y;X+Y(NO3)2===X(NO3)2+Y;Z+H2SO4(稀)===ZSO4+H2↑ X跟稀H2SO4不发生反应.则三种金属的活动性由强到弱的顺序是__________________.
13.X、Y、Z三种金属的活动性,可用下列化学方程式说明:Z+Y(NO3)2===Z(NO3)2+Y;X+Y(NO3)2===X(NO3)2+Y;Z+H2SO4(稀)===ZSO4+H2↑ X跟稀H2SO4不发生反应.则三种金属的活动性由强到弱的顺序是__________________.
【考点4】根据不同金属与酸溶液反应的图像关系,判断生成氢气的速率、质量、金属活动性顺序并比较相对原子质量的大小
14.等质量的两种常见的金属A、B(二者在化合物中呈现的化合价相同)与足量的盐酸反应,那么在反应时间0~t1之间时,生成氢气的速率A_______B,A、B的金属活动性顺序为A________B,A、B最终生成氢气的质量A________B,A、B相对原子质量A______B。
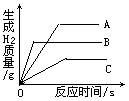 15.将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示。根据图中所提供的信息,得出的结论正确的是。(已知:A、B、C在生成物中均为+2价)
15.将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示。根据图中所提供的信息,得出的结论正确的是。(已知:A、B、C在生成物中均为+2价)
A.放出H2的质量是A>C>B B.金属活动性顺序是A>B>C
C.反应速率最大的是A D.相对原子质量是C>B>A
16.将质量相等的铝粉和铁粉分别与同体积、同浓度的稀硫酸反应。反应情况如图5所示。有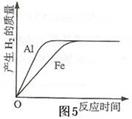 关叙述中正确的是( )
关叙述中正确的是( )
A.铝粉、铁粉和硫酸均有剩余
B.铝粉、铁粉均反应完,硫酸有剩余
C.硫酸、铝粉均反应完,铁粉有剩余
D.硫酸、铁粉均反应完,铝粉有剩余
以下内容供成绩较好的同学使用
【考点5】考查金属与盐溶液之间的置换反应(较难)
★知识链接:金属与盐溶液发生置换反应的条件是:
(1) 金属的位置:只有排在前面的金属才能把后面的金属从其盐溶液中置换出来;
(2) 特殊性:由于钾、钙、钠的化学性质非常活泼,在盐溶液中它们首先会与水反应生成相应的碱和氢气,因而不会置换出盐中的金属;例:钠投入硫酸铜溶液中发生的化学反应为:![]() ↑,
↑,![]()
(3) 盐必须溶于水;(4) 铁与盐溶液反应时生成+2价的亚铁盐,金属与铁盐反应时要用+2价的亚铁盐;,例![]()
(5)同一金属与不同的盐反应时, 该金属先与活动性较弱的金属所组成的盐反应;不同金属与盐溶液反应时,活动性强的金属先与盐反应,或者说:金属活动性相差越大,置换反应越易发生。
17.在Cu(NO3)2和AgNO3的混合溶液中,加入一定量的锌粉,充分反应后过滤,留在滤纸上的物质中一定含有 A.Cu B.Ag C.Cu、Ag D.Zn、Ag
18.向含有Fe、Cu粉组成的混合物中加入一定量的硝酸银溶液,充分反应后过滤,向滤渣中滴加稀盐酸有气泡产生。则滤出的固体中一定含有的金属是下列的:
A.Ag B.Ag、Fe C.Ag、Cu D. Ag、Cu、Fe
19.向AgNO3、Cu(NO3)2和Mg(NO3)2混和溶液中加入过量 铁粉,充分反应后溶液中含有的大量金属离子是( )
A.Ag+、Cu2+、Mg2+ B.Cu2+、Mg2+、Fe2+ C.Cu2+、Fe3+、Mg2+ D.Mg2+、Fe2+
20.向AgNO3、Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后有金属析出,过滤、洗涤后向滤渣中加入稀盐酸,有无色气体放出,则滤液中一定存在的物质是
A.Fe(NO3)3 B.Cu(NO3)2、Fe(NO3)2 C.Fe(NO3)2 D.AgNO3、Cu(NO3)2、Fe(NO3)2
21.(难题)某金属加工厂生产过程中的废液含有少量Cu(NO3)2和AgNO3,为回收利用资源和防止污染,该厂向废液中加入一定量的铁粉,反应停止后过滤,向滤出的固体中加入少量稀盐酸,无气体产生。则下列有关说法中,正确的是( )
A. 滤出的固体中一定含有银和铜,一定不含铁
B. 滤出的固体中一定含有银,可能含有铁和铜
C. 滤液中一定有硝酸亚铁,一定没有硝酸银和硝酸铜
D. 滤液中一定有硝酸亚铁,可能有硝酸银和硝酸铜
【考点6】考查反应后溶液质量的变化情况(较难)
★知识链接:判断置换反应发生后溶液质量的变化,只要比较反应前后溶液中溶质的相对分子质量与相应计量数的积的大小即可。若反应后的溶液中溶质的相对分子质量与相应计量数的积变小,则反应后溶液的质量减小,否则增大。
22.把铁片分别放入下列各物质的溶液中,片刻后取出,溶液质量增加的是( )
A .Al2(SO4)3
B.CuSO
23.有X、Y、Z三种金属,把Y投入XCl2溶液中,Y溶解后溶液的质量增加;把X投入Z(NO3)2溶液中,X溶解后溶液的质量减少。下列判断正确的是
A、金属活动性顺序:X>Z>Y B、相对原子质量:Y>Z>X
C、X、Y、Z可能依次是Hg,Zn,Cu D、X、Y、Z可能依次是Cu,Zn, Hg
24.下列各组中的两种物质,混合后过一段时间,溶液质量减少的是( ).
A.铁片和氯化镁溶液 B.锌片和硫酸铜溶液
C.铝片和稀硫酸 D.铜片和硝酸银溶液
25.下列盐溶液,投入铁片反应后,使溶液质量减轻的是 [ ]
A.MgSO4 B.Zn(NO3)2 C.Cu(NO3)2 D.AlCl3
【考点7】金属与酸反应产生氢气的能力大小比较
![]()
或![]()
26.两种金属粉末的混合物30g与足量的稀硫酸反应生成1g氢气,则这种混合物的可能组成是
A、Fe和Mg B、Fe和Al C、Mg和Al D、Zn和Fe
注意:Al 要折算为二价铝,即27×2/3===18为铝的对应量。若Na折算为二价应为23×2
27.有20.75g由两种金属粉末组成的混合物,将它投入到足量的盐酸中,充分反应后,收集到1g氢气。混合物可能的组成是:(注意铜不与盐酸反应)
A、锌和铁 B、铜和锌 C、镁和铜 D、锌和铝
28.3g含有一种杂质的铁粉跟足量稀硫酸反应,生成0.1g氢气,该杂质不可能是:
A、Cu B、Al C、Mg D、C
29.有一不纯的铁5.6g与足量的盐酸反应,放出0.18g氢气,则铁片中可能含有的一种金属杂质为 A、Cu B、Al C、Mg D、C
30.有一包不纯的铁屑,取5.6克该铁屑放入到足量的稀硫酸中,完全反应,且无固体剩余,放出0.18克氢气,则铁屑中可能含有:A、Mg B、Al C、Zn D、Cu
31.锌、铁、镁的混合物4g,与足量的稀硫酸完全反应,蒸发水份后,得到固体物质为13.6g,试计算生成的氢气的质量?
A.锌最多,铁最少 B.铝最多,锌最少 C.铁最多,铝最少 D.一样多
【考点8】关于天平平衡问题:
32.在托盘天平的两边各放一只盛有足量相同质量、相同质量分数稀盐酸的烧杯,调至平衡,然后向左边烧杯中加⒌6g铁,欲使天平再次保持平衡,应向右边烧杯中加入:
A.6 g镁 B.⒌6 g铜 C.⒌4 g氧化钙 D.10 g碳酸钙
33.把盛有等质量盐酸的烧杯,分别放在天平托盘上,天平平衡后,将铝粉放入左杯,镁粉放入右杯,充分反应后酸仍足量,如果使天平仍保持平衡,则加入铝镁两种金属的质量比是
A.24∶27 B.27∶24 C.33∶32 D.32∶33
通讯地址: 广州市天河区东圃黄村龙怡苑 (510660)邮箱:lzm6308@163.com 联系QQ:534386438
Copyright © 2008-2012 klxkc.com All Rights Reserved. 粤ICP备15026984号-1

