| �ϴ���gxda147369 | ��˷�����admin | ����ʱ�䣺2015-10-12 18:58:36 | ���������477�� |
���꼶��ѧ�����п��Ի�ѧ�Ծ�����������
1������ʮ�˴��а�����̬�����������״����������ߵ�ս�Բ��棬Ҫ��Ӵ���Ȼ��̬ϵͳ�ͻ����������ȡ�����������������һҪ�����
|
A���������������Դ |
B��ȫ���ͣ������ҵ |
|
C���Ľ�����β���������� |
D���з����������ũҩ������ |
���𰸡�B
��������
���������A��C��D���������ڻ���������������B��ȻҲ�����ڻ�������������������ʵʩ����Ϊ������ҵ��ϵ�������������ȷ������棬����ȫ��رգ�ֻ�ܹرղ��ָ���Ⱦ����ҵ���ֻ�����ҵӦ�þ����������ۣ����Ż����Ѻõķ���չ��
���㣺��������
2������������в����У������˻�ѧ�仯����
|
A�������� |
B��ĥ���� |
C���лƹ� |
D������ |
���𰸡�D
��������
�����������ѧ�仯ָ���������ʵı仯��A��������ֻ������ɷ�ĩ״���˿״����û���������ʡ�B��ĥ����ֻ�Ƕ���״̬�����仯���ɿ�״��ɷ�ĩ״��û�в��������ʡ�C���лƹ�ֻ�ǻƹ��ɿ�״��Ƭ״��Ҳֻ��״̬�����仯��û���������ʡ�D�������������ʾƾ����ɣ����ڻ�ѧ�仯��
���㣺��ѧ�仯�б�
3�������г��Ӵ������ӵ�ʳ���������߸�ţ���������е���������������Ӧ����Ϊ
|
A������ |
B������ |
C��Ԫ�� |
D��ԭ�� |
���𰸡�C
��������
������������ӵ�ʳ���������߸�ţ�������Ǻ�����ʣ���������Ԫ����ɵġ��ʵ⡢�ƶ���ָԪ�أ�C��ȷ��B��D������ЩԪ�ض����Ի�������ʽ���ڵģ���A����
���㣺���ʡ�Ԫ�ء����ӡ�ԭ��֮��Ĺ�ϵ
4���������ʼ��ǿ����ijɷ֣����������������
|
A�������� |
B������ |
C��ˮ���� |
D��ϡ������ |
���𰸡�C
��������
��������������ijɷ��в���������������A�϶�������������Ķ��壺������Ԫ����ɵĻ��������һ��Ϊ��Ԫ�ء�ʣ������������������������ֻ��C��
���㣺�����ɷ֣��������б�
5������ʵ������У���ȷ����
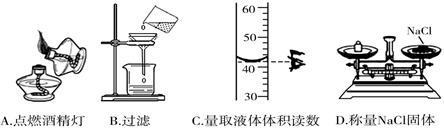
���𰸡�C
��������
���������A����ȼ�ƾ���ʱ�����þƾ�����ȼ��һֻ�ƾ��ƣ�����B�����˲���ʱӦ������һ�������͡���������ЩҪ�����������´���Ӧ�ò�������������ֽӦ����©����Ե��©���¿�Ӧ�����ձ��ڱڣ�ʹ��Һ���ձ������¡�����C����ȷ������ʱ����������Ͳ��Һ�尼Һ����ʹ�����ˮƽ����ѡC��D������ƽ����ʱ��Ӧ������������̣���������̡�����
���㣺��ѧʵ���������
6���÷��ӡ�ԭ�ӵĹ۵�������������е���������Ͳ���������
|
ѡ�� |
���� |
���� |
|
A |
50mLˮ��50mL�ƾ���Ϻ������С��100mL |
����֮���м�� |
|
B |
���¹��� |
�����ڲ����˶� |
|
C |
1��ˮ��Լ��1.67��1021��ˮ���� |
���Ӻ�С |
|
D |
ˮ��� |
���Ӳ������������� |
���𰸡�D
��������
���������A����ȷ����Ϊ���Ӽ��м������Ϻ�ˮ�����굽�˾ƾ����ӵĿ�϶�У���ʹ�������100С��B����ȷ�����Ӵӹ��˶������˵ı��ӡ�C����ȷ��һ��ˮ�������С����ôС��һ��ˮ�л�����ô������ӣ��ɼ�ÿ�����ӵ�������������dz�С��D��ˮ�����һ����ѧ�仯����ѧ�仯�ı����Ƿ��ӵ����Ѻ�ԭ�ӵ�������ϡ��ñ仯�У�ˮ���ӱ�ɵ�����Ӻ������ӣ����ӷ����˸ı䣬D����
���㣺�÷��ӡ�ԭ�ӵĹ۵���������е�����
7�����к�����Ԫ�ص������У���Ԫ�صĻ��ϼ���ߵ���
|
A��H2SO3 |
B��H2SO4 |
C��KHSO3 |
D��Na2S2O3 |
���𰸡�B
��������
������������ݻ������У��������ϼ۴�����Ϊ0��ԭ�ֱ��������Ԫ�صĻ��ϼۣ��ٽ��бȽϼ��ɡ�������Ԫ�ػ��ϼ�ΪX��A��(+1)��2+X +(-2)
��3=0�����X=+4��B��(+1)��2+X +(-2) ��4=0�����X=+6��C��(+1)+ (+1)+X +(-2) ��3=0�����X=+4��D��(+1)��2+2X
+(-2) ��3=0�����X=+2�����ϼ���ߵ���B��
���㣺���ϼۼ���
8�����б仯�����ڻ�����������
|
A������ȼ�� |
B��ʳ�︯�� |
C���������� |
D��ֲ����� |
���𰸡�A
��������
�������������������ָ���еĺܻ�����������Ӧ������ȼ�գ���Ӧ�ܾ��ң������⣬�ų������ȣ�����A�����ڻ���������
���㣺����������ȼ�յ��б�
9���������ʲ���Ϊ������Ⱦ����롶��������������������������
|
A��CO2 |
B��SO2 |
C��CO |
D��PM10��PM2.5 |
���𰸡�A
��������
���������������Ⱦ�����������������������һ����̼�������弰�������������ڽ�����Ҳ��Ϊ������Ⱦ��������������Ԥ����Χ��Dѡ���е�PM10��PM2.5��ֱָ��Ϊ10��2.5�Ĺ����������ڿ����������ķ�Χ������������֪������ѡA��
���㣺������Ⱦ��
10������ͼ��ʾ�ļ���ˮ���������ǵĺ�ˮ�����������ȷ����
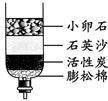
|
A����ˮ����ɱ������ |
|
B���������ˮ���ڴ����� |
|
C��С��ʯ��ʯӢɳ�����ö��ǹ��� |
|
D����ˮ���ܽ�Ӳˮ��Ϊ��ˮ |
���𰸡�C
��������
�������������ˮ����װ��С��ʯ��ʯӢɳ������̿�����ʾ��й������ã���ȥˮ�еIJ����Թ������ʣ�����̿�������������ã��ܳ�ȥˮ�е�ɫ�ء���ζ�ȣ������þ�ˮ�������ĺ�ˮ��ֻ�dz�ȥ���������ʣ���ˮ�к��е�һЩ���������ʣ�������Ը�þ��������dz������ģ�Ҫ��ȥ�����Ը�þ�����ֻ�ܲ�����л�����ķ�����ˮ�еIJ�����Ҳ��ɱ�����ʴ�ѡC��
���㣺����ˮ����ˮԭ��
11�������Ļ�ѧ���ʱȽϻ��ã�����������ʷ�Ӧ�����ж��йط�Ӧ��������ȷ����
|
A���ڵ�ȼ�������£�ϸ��˿�������о���ȼ�գ��������䣬���ɺ�ɫ������������ |
|
B���ڵ�ȼ�������£�����������ȼ�գ���������ɫ���棬������ɫ��ζ������ |
|
C��������ʯ���������е�ȼ�ն��ǻ��Ϸ�Ӧ |
|
D�����������������ķ�Ӧ����������Ӧ���������������� |
���𰸡�D
��������
���������A����˿��������ȼ�գ����ɵĺ�ɫ���ʲ�����������������������������������B����ȼ�գ����ɵ��������д̼�����ζ�ģ�����C����������������ȼ�գ������ﶼֻ��һ�֣�ȷʵ���ڻ��Ϸ�Ӧ����ʯ��ȼ�գ��������ж�����̼��ˮ���֣������ϻ��Ϸ�Ӧ�Ķ��壬����D��������Ӧ���������������ķ�Ӧ���������������ʼ�������Ҳ�����ǻ������е�����Ҳ����˵�����������������ķ�Ӧȷʵ����������Ӧ������Ҳ�Ǿ��������Եģ�������������õ���������D��ȷ��
���㣺������������ȼ�յ�����
12�����������У����������ӵ���
|
A��O2 |
B��Na2O2 |
C��SO2 |
D��NO2 |
���𰸡�A
��������
�����������������һ�ֵ��ʷ��ӣ�ֻ����Ԫ��һ��Ԫ�أ���Ϊ˫ԭ�ӷ��ӡ��ʴ�ѡA��
���㣺��ѧʽ��д
13������ʵ�鷽�����ﵽʵ��Ŀ�ĵ���
|
A���ó���ʯ��ˮ���������Ͷ�����̼ |
B����ȼ�ŵ�ľ���������������̼ |
|
C���ô����ǵ�ľ�����������Ϳ��� |
D��������ͭ��Һ����ˮ����������Һ |
���𰸡�B
��������
������������ʵļ����Ǽ���ij�Լ���������ͬ��ʵ�������ݲ�ͬ����������ѧ���Ļ�ѧ֪ʶ�������������ж������֡�A���������ʯ��ˮ��ʯ��ˮ����ǵ��Ƕ�����̼��û����ǵ����������������֡�B���������嶼��ʹȼ�ŵ�ľ��Ϩ�������֡���ѡB��C��������ľ�����룬��ȼ����������û���Ա仯���ǿ������������֡�D����������ͭ��Һ���д������ݲ������ǹ���������Һ����Ϊ����ͭ��Һ�ǹ�������ֽ�Ĵ�������û���������ˮ���������֡�
���㣺���ʵļ���
14����ѧ�Ҵ����һ����������ˮ���� ��ÿ��������ˮ95���������SiO2 ����ˮ���ն�����̼����������ͨ��ˮ�������������й�˵����ȷ����
|
A����ˮ�ͱ���ͬһ������ |
B����ˮ�е�ˮ���Ӳ����˶� |
|
C���ø�ˮ����CO2�����ڼ�������ЧӦ |
D��ͨ������£���ˮΪҺ̬�� |
���𰸡�C
��������
���������A������֪����ˮ���ڻ�����ɷ�Ϊˮ�Ͷ������裬�����ijɷ�Ϊˮ�����Ը�ˮ�ͱ�����ͬһ�����ʡ�����B�����������ڲ����˶��ġ�����C������ЧӦ��Ҫ���ɶ�����̼����ģ���ˮ��������̼���գ������ڻ�������ЧӦ����ȷ����ѡC��D�����ڸ�ˮ���Ϊ�������裬����������һ�ֹ������ʣ�����ͨ������£���ˮΪ��̬������
���㣺���ӵ����ʣ����������״̬����������ЧӦ��ԭ��
15�����л�ѧ������д��ȷ����
|
A�������ԭ��-��H5 |
B������ˮ���ӣ�3H2O |
|
C�����������ӣ�2Ca+2 |
D���ĸ�笠����ӣ�4NH3+ |
���𰸡�B
��������
���������A����ԭ����H��ʾ�����Ӹ���Ӧд�ڷ���ǰ�棬��ȷд��Ӧ����5H��B����ȷ����ѡB��C�����ӷ�����дʱ��Ӧ�����Ͻ���д���֣���д�����š���ȷд��Ӧ����2Ca2+��D��笠���д��Ӧ����NH4��NH3�ǰ�������ȷд��Ӧ����4NH4+��
���㣺��ѧ�������д
16��2013��1��19�գ��������ʷ��ι���Ⱦ��Լ����������ͼΪԪ�ع�����Ϣ����ͼ�л�õ���Ϣ��ȷ��һ����
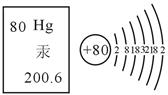
|
A�������ڷǽ���Ԫ�� |
|
B�����ĺ˵����Ϊ80 |
|
C���������ԭ������Ϊ200.6g |
|
D���ڻ�ѧ��Ӧ�У���ԭ�����õ����� |
���𰸡�B
��������
���������A�����ĺ��ֽṹ����û�н����ԣ���ȴ�ǽ���Ԫ�ء�����B�����������Ͻǵ����ֱ�ʾ����ԭ������������ֵ����ԭ�ӵĺ˵������Ҳ������������Ҳ����ԭ�Ӻ������������ȷ��C���������·������ֱ�ʾ���ԭ�������������ԭ�������ĵ�λ���ǿˣ�������1����ͨ��ʡ�Բ�д������D�����ݹ�ԭ�ӽṹʾ��ͼ���������Ϊ2�����ӣ���4С���ڷ�Ӧ����ʧȥ�������ӣ�����
���㣺Ԫ�����ڱ�ÿ����������ֻ��������ʾ����Ϣ��ԭ�ӽṹʾ��ͼ��ʾ����Ϣ
17���������������ӹ��ɵ���
|
A��ˮ |
B������ͭ |
C������ |
D��C60 |
���𰸡�B
��������
���������ˮ��C60�����ɷ��ӹ��ɵģ���������ԭ�ӹ��ɵġ�����ͭ����ͭ���Ӻ���������ӹ��ɵġ��̲��о����ᵽ�������ӹ��ɵ��������Ȼ��ƣ����������Ӻ������ӹ��ɡ�
���㣺���ʵĹ���
18�����������У������ڱ���ˮ��Դ����
|
A��ʹ�ý�ˮ����Ͱ |
B������ʹ��ũҩ�ͻ��� |
|
C��������ˮ�����ŷ� |
D����ҵ��ˮ���������ŷ� |
���𰸡�C
��������
�������������ˮ��Դ��Ϊ�����棬һΪ��Լ��ˮ����Ϊ��ֹˮ����Ⱦ��A���ڵ�һ���棬BD���ڵڶ����档
���㣺����ˮ��Դ��ʩ
19��ij��Ӧ����ʾ��ͼΪ��

���д�ͼ������õ���Ϣ�У���ȷ����
|
A��ͼ�������ֲ�ͬ�������� |
B����Ӧǰ����ӵ������ |
|
C����Ӧ������û�е������� |
D����Ӧǰ���Ԫ�ػ��ϼ۲��� |
���𰸡�A
��������
���������A����������ָ������Ԫ����ɵĻ��������һ��Ϊ��Ԫ�ء�ͼ�д�����1��3�������ʷ���Ҫ��A��ȷ��B����ѧ��Ӧ�ı����Ƿ��ӵ����Ѻ�ԭ�ӵ�������ϣ���ѧ��Ӧ�з��ӵ�����һ���ᷢ���仯������µķ��ӡ���B����C��������ָͬ��Ԫ����ɵĴ����ͼ�е�4�������ǵ��ʣ���C����D����ͼ�п�������Ӧǰ̼Ϊ���ʣ���Ӧ�����˻�����CO��̼Ԫ�صĻ��ϼ���0���+2�����⣬��Ԫ�صĻ��ϼ�Ҳ�����˸ı䣬��+1�����0����D����
���㣺�����������б���������ʼ���ѧ��Ӧ
20����ͼ��ʾ����������˵����ȷ����
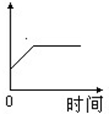
|
A��ͼ��ʾ�����������Һ����������MnO2��Ӧ����������O2��������ʱ���ϵ |
|
B��ͼ��ʾ�����������Һ����������MnO2��Ӧ��������Һ��ˮ��������ʱ���ϵ |
|
C��ͼ��ʾһ����KMnO4������ȡO2�����У�����������MnO2��������ʱ��Ĺ�ϵ |
|
D��ͼ��ʾ����˫��ˮ�Ͷ��������Ʊ������ķ�Ӧ������MnO2�������仯��ϵ |
���𰸡�B
��������
�����������ѧͼ��ʶ��һ��Ӧ�ÿ���㡢�յ�ͱ仯�����������档A����㣺��ͼ�Ͽ�������Ӧʱ��Ϊ0��ʱ�������꣨��������������������һ������������ʵ�ϵ���Ӧʱ��Ϊ0��ʱ��������������Ҳ��0���ʵ�����㿴��A�����ϸ�ͼ�����Ҫ���ϣ�Ӧ��ͼ�е���������������ƽ�ƣ�ֱ���ߵ������ֱ������ϵ��ԭ���ϡ�B����㣺������ʱ��Ϊ0��ʱ�������꣨��Һ��ˮ������������һ������������ʵ��Ҳȷʵ��ˣ���Ӧ��û��ʼ��ʱ����������Һ�о�����һ������ˮ���ڣ�����㿴������Ҫ�յ㣺��ν�յ���ָ����ͻȻ�����仯�ĵ㡣��ϱ仯���Ʒ������£����ŷ�Ӧ�Ľ��У�����ˮ����Խ��Խ�࣬ͼ�ϱ���Ϊֱ�����ϱ仯��������Ӧ���е����ʱ��ˮ������ͻȻ�������࣬���DZ���ԭ�е�ˮ���������䣬ͼ�ϱ���Ϊֱ��ƽ��������꣬��ֱ�����ϱ仯��ֱ��ƽ��������꣬��Ȼ����һ���յ㡣��B���ϸ�ͼ����ѡB��C������㿴����ͼ�����ϣ���Ϊ��Ӧʱ��Ϊ0��ʱ���������ж������̵�����ҲӦ����0�����Ҫ���ϣ�Ҳ�ý��������������Ƶ����Ϊֱ������ϵ��ԭ�㡣D��˫��ˮ��ȡ����ʱ������������Ϊ������ʹ�õģ����������������ı䣬ͼ��Ӧ����Ϊ�Ǵ����ҵ�һ��ƽ���ں������ֱ�ߣ�����㲻��ֱ������ϵ��ԭ���ϣ���Ϊ��Ӧʱ��Ϊ0��ʱ�������̾�����һ���������ˡ���D����
���㣺��ѧͼ���ʶ��
21����ѧ�����������ߣ��������ǵ�����ϢϢ��ء�
��1������H��N��O��Ne���ֳ�����Ԫ�أ���ѡ�����е�Ԫ��д����������Ҫ������ʸ�һ�֣��û�ѧʽ��ʾ��
�����������ֵ������� ������Է���������С���������� ��
��ͨ�緢���������� ���������к����������� ��
��2���ճ������еIJ�����Ʒ��ˮ���йأ����¼ƾ�������֮һ��С��ż����ð��������ʱ��С�Ľ����¼ƻ���ˤ�飬������ɢ������ˮ���顣С�����룺ˮ���ж���������������������Ѱ��С����ȡ�����й�ˮ�������ϣ�ˮ��ѧ��Ϊ������������������ɫҺ�壬���ܶȴ������������������ر�ã���������ˮ�����������Ĵ�����������ж������ڻ������г�����Ϊ+2�ۣ���������Ӧ���ɲ�������ˮ��������������������������Ϣ����ش��������⣺

������ˮ���������ʵ��� ��ѡ����ţ���
��ˮ������ ���ɣ������ӷ��ţ���
��������Ӧ�ķ��ű���ʽ ���÷�Ӧ�����е���С������ �������ӷ��ţ���
���𰸡�
��1����O2 ��H2O ��Ne ��N2
��2���٢ڢۢ�
Hg ����+������ Hg��S
��������
�����������1������������;�ǹ���������֧��ȼ�գ���������֧��ȼ����һ��Χ������Է���������С����������ˮ����������뺬��Ԫ�أ�����һ��Ԫ�ص����ԭ����������Ҫ������С��������ɵ����������Է�������������С����һ��Ԫ��һ������Ԫ�أ�û��˭�����ԭ�����������С�ˣ����Ը�������Ϊ��������ɵ�ˮ��������⣬��Ȼֻ��ѡ�����е�ˮ����ͨ��ᷢ����ɫ�����ϡ�����壬����ֻ�����������������к��������ǵ�����ռ�����������78%��
��2��������������ָ����ͨ����ѧ�仯���ֳ��������ʣ�����ɫ̬ζ���۵㡢�е㡢Ӳ�ȡ��ܶȼ��ܽ��Եȡ��������٢ڢۢ�����Ҫ����ˮ���ǽ���������ԭ��ֱ�ӹ��ɣ�����д��ԭ�ӵķ���Hg����������Ŀ��Ϣ���ɵó���Ӧ��Ϊ������������Ϊ������Ӧ����û����ȷָ������Ϊ��ͨ������£��ʱ���ʽд�ɣ���+�� ���� ���û�ѧ��Ӧ�е���С������ԭ�ӣ�������ԭ�ӣ�Hg������ԭ�ӣ�S����
���㣺��ѧʽ����д���������ʵ��б����ʵĹ��ɣ���Ϣ����ʽ����д��ԭ�Ӹ��������
22��д�����з�Ӧ�ķ��ű���ʽ������������ע����Ӧ�Ļ������͡�
��1����˿��������ȼ�� ���� ����
��2�����Ȱ���ɫ������ȡ���� ���� ����
��3��ľ̿�ڿ�����ȼ�� ��
��4�������������������������֮�佨����ϵ���ǻ�ѧѧ�����е�˼ά��ʽ��ij��ѧ��Ӧ����ģ��ʾ��ͼ���£�
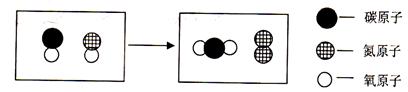
�÷�Ӧ�ķ��ű���ʽ�� ��
���𰸡�
��1��Fe+O2![]() Fe3O4 ����
Fe3O4 ����
��2��KMnO4![]() K2MnO4+MnO2+O2 �ֽ�
K2MnO4+MnO2+O2 �ֽ�
��3��C+O2![]() CO2
CO2
��4��CO+NO��CO2+N2
��������
�����������2������ɫ����ָ������أ�������ǰ�ɫ���壬������������ɫҺ�塣 ��4�������Ҳ�ͼ�������Dz��ѵó�����Ӧ��ΪCO��NO��������ΪCO2��N2��
���㣺��ѧ���ű���ʽ����д����Ӧ���͵��б������ӵ���ʶ
23��ijͬѧ��ͼװ�òⶨ�����������ĺ�����
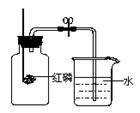
��1������ȼ�յ������� �����ȣ���Ӧ�ķ��ű���ʽ ��
��2����ijͬѧ�ó��Ľ��ۣ����������������Լռ1/5���ܵó��˽��۵�ʵ������Ϊ ��
��3��С����������ͼ��ʾװ�ò����������������������ȡ�óɹ���
[��������]�����Ż��40����
[ʵ����]��ƿ�ڿ������Ϊ230mL��ע������ˮ�����Ϊ50mL����װ�����������á�
[ʵ��̽��]װ��ҩƷ����ͼ��ʾ���Ӻ��������н����ɼС��Ƚ���ƿ�ײ�������ˮ�У����ܿ챻��ȼ��Ȼ����ƿ����ˮ��ȡ����
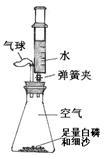
[�������]
������ƿ�ײ�������ˮ�У����ױ���ȼ��
��������ʵ������У��ɹ۲쵽����ı仯�� ��
��������Ϩ����ƿ��ȴ�����º��ɼУ����ɹ۲쵽������һ�ǣ�ע�����е�ˮ�Զ����������ԭ���� ��������ǣ���ע�����е�ˮ��ʣԼ4mLʱֹͣ���¡����ñ�Ҫ������˵��ԭ�� ��
���𰸡�
��1�������������� P+O2![]() P2O5
P2O5
��2������ƿ��ˮ������Լ���������������֮һ
��3�����ȱ��ָ�ԭ����������ȼ�գ�������ƿ�е��������ģ���ѹ���٣���ˮ�����롣���������������ƿ���Ϊ230mL������ȼ�ս�����Լ���֮һ���������ģ������ռ46mL��ע�����е�46mLˮ�ͻᱻ���뼯��ƿ��ע������ʣ��ˮ�������ԼΪ50-46=4mL
��������
�����������2����������������ж��٣�������ֱ�ӹ۲쵽��ֻ��ͨ�������滻�����Ʋ⣬�����������ģ�����ˮ�������ʧ�������������ͨ���۲�ˮռ��������Ķ��٣������֪����ռ������١����Դ�Ϊ����ƿ��ˮ������Լ���������������֮һ��
���㣺���������������ⶨ��ʵ��Ľ�
24���±���Ԫ�����ڱ���һ���֣�
|
�� |
IA |
|
0 |
|||||
|
1 |
1 H |
��A |
��A |
��A |
V A |
��A |
��A |
2 He |
|
2 |
3 Li |
4 Be |
5 B |
6 C |
7 N |
8 O |
9 F |
10 Ne |
|
3 |
11 Na |
12 Mg |
13 |
14 Si |
15 P |
16 S |
17 Cl |
18 Ar |
��1���ؿ��к������Ľ���Ԫ�ط��� �������ں�����ߵ�Ԫ������ �� ��1��8��12������Ԫ����ɻ�����Ļ�ѧʽ ��
��2�����ԭ������Ϊ35.45��Ԫ���� �����������������ǽ�������Ԫ�أ����ڷ�Ӧ������ �������õ�������ʧȥ�������ӣ���Ԫ������������Ϊ ���������仯ѧ�������Ƶ�Ԫ���� ��
��3�����в�ͬ��Ԫ����ʵ������� (�����)
A����������ͬ
B�����ԭ��������ͬ C����������ͬ
��4��д����������Ų�����ԭ����ͬ�������Ӻ������ӷ��Ÿ�һ���������ӷ��ţ������� �������� ��
���𰸡�
��1��Al �� Mg(OH)2
��2���ǽ��� �õ� 2 �ʺ��
��3��A
��4��Na+ O2-
��������
���������(1)�ؿ��к�������Ԫ������Ϊ�����衢������������������Ϊ�ǽ�����������Ϊ�����������к�������Ԫ������Ԫ�ء�1��8��12����Ԫ�طֱ�Ϊ�⡢����þ��������3�ֻ�����Ԫ����ɻ����һ���Ȱ����е��������ԭ���ţ�Ȼ�����������Ԫ�ؽ���γɻ������д��ѧʽʱ��Ӧ������Ԫ�ط���ǰ�棬����Ԫ�ط��ں��档���Դ�ΪMg(OH)2��
��2��ÿ�������·������ֱ�ʾ���ԭ�������������֪���ԭ������Ϊ35.45��Ԫ������Ԫ�أ����Ƿǽ���Ԫ�ء������ȵ�����������Ϊ7����4���ڷ�Ӧ���õ������γ��ȶ��ṹ��Ԫ�صĻ�ѧ������������������ϵ���С���������������Ϊ2�������ж�����Ӳ�������Ϊ8�����ӵĽṹһ�����������ȶ��ṹ������˵���ڱ���ͬһ�����е�Ԫ�ػ�ѧ���ʶ������Ƶġ��ʴ�Ϊ�ʺ�벡�
��3��Ԫ���Ǿ�����ͬ�˵����������������һ��ԭ�ӵ��ܳơ��ɶ���֪��ֻҪ�˵��������������ͬ����һ��ԭ�Ӿ�����ͬ��Ԫ�ء����Բ������⣬Ԫ����Ԫ����ʵ�����������������ͬ��
��4����ԭ�ӵĺ����������Ϊ��һ��2�����ڶ���8������������ԭ��ʧȥ�����γɵģ��Ǹ�ԭ��Ӧ����3�����Ӳ㣬�ҵ�3���ϵĵ�����С��4�����Է��ϴ𰸵��������ӡ�þ���ӡ������ӵȡ���������ԭ�ӵõ������γɵģ��Ǹ�ԭ��Ӧ����2�����Ӳ㣬��������ϵĵ���������4������Ҫ����������ӡ������ӵȡ�
���㣺Ԫ�����ڱ���ԭ�ӽṹʾ��ͼ�����ӷ��ż���ѧʽ����д�ȡ�
25��ˮ������֮Դ��������ճ������빤ũҵ�������벻��ˮ����Ȼ���ˮ����ֱ��ʹ�ã�����Ҫ����������ʹ�á�������ѧ֪ʶ�ش��������⡣
��1�����Ե���������ˮת��Ϊ������ˮ�IJ����У�
�����������л�ѧ������ ����Ư������ɱ���� �����ˣ� ��������С�
���������������йز��������˳���� ������ţ���
��2���������ˮ���н϶�ĸơ�þ���ӣ�����ˮ��Ӳˮ������ֱ�����á���������ѧ֪ʶ��֤��ij���еĵ���ˮ��Ӳˮ�������� ��
��3��ˮ����Ȼ�����в��ֽ⣬����ͨ��������¿��Էֽ⣬д���÷�Ӧ�ķ��ű���ʽ ������ͼ��ʾ��װ���У�����Դ��ͨһ��ʱ����������������ҹ�����������֮��Ϊ ��
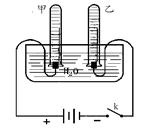
���𰸡�
�Ţ٢ۢڢ�
��ȡ���������м��������ķ���ˮ���裬�����϶�ĸ�������Ӳˮ��
��H2O![]() H2��O2
1 �U 2
H2��O2
1 �U 2
��������
�����������1����ν������˳����ָ����ˮ��Ч���ɲ�����С���������ѧ��������������ˮ�е�С�����������ʣ�����Щ�����������������ײ���ֻ����ˮ�ֲ㣬��û�з��룬��Ч���������ܳ�ȥ�������ʣ��õ���ˮ�в��ٺ����壬�������������Ը�þ������Ȳ�û�г�ȥ����Ч����֮����Ư������ɱ����ȥ������������Ч��û�м�����кã�������г��ɳ�ȥ�����⣬���ܳ�ȥ���ֻ�ȫ�������Ը�þ�����
��2��Ӳˮ�ļ����Ǽ������ˮ���裬�۲���û����ĭ��������ԭ�������÷����ijɷ�Ӳ֬����������þ����������ֽⷴӦ�����������Ե�Ӳ֬��ơ�Ӳ֬��þ�γɳ���������ν�ĸ����������Կ����и�������ζ�Ÿ�ˮΪӲˮ��
���㣺ˮ�ľ�����Ӳˮ�ļ��飬���ˮʵ��
26�������Ǽ���ʵ������ȡ����ķ���װ�ú��ռ�װ�á���ش��������⣺
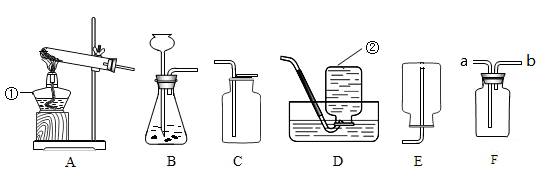
��1��ָ��ͼ�б������������������� ��
��2��ʵ������˫��ˮ�Ͷ���������ȡ���ռ���Ϊ����������ѡ�õ�װ���������ǡ�ijС��ͬѧʹ�õ�ʵ��װ�������Ժܺã���������������������ð��ʱ��ʼ�ռ����������ռ�����������������ʼ����95%���ң��Է���ԭ������� ��
��3��F��һ�ֿ�����ϴ���������ȶ��ֹ��ܵ�װ�á�Сǿ���ü�������صķ�����ȡ�ϸ������������Ӧѡ������װ���е�A��F������װ��д���÷�Ӧ�ķ��ű���ʽΪ ������ʱ�Թܿ�Ҫ��������б��ԭ���� �������ķ����� ��
��4��ʵ����Ҳ����Aװ���Ʊ����飨CH4�����壬�Ʋ��䷴Ӧ���� ������ţ���
A�������ƺͼ�ʯ�ҵĹ������� B��Na2CO3�����ˮ C��CO2��H2
���𰸡�
�Ţ�����ƿ
��BD����ˮ���ռ��������к���һ����ˮ����
��KClO3![]() KCl��O2
KCl��O2
��ֹ����ˮ�������ȵ��Թܵײ���ը���Թܡ�
�������ǵ�ľ�����ڵ���b�����۲��Ƿ�ȼ������ȼ����������
�� A
��������
�����������2�����巢��װ�÷����֣��̹̼����ͣ�A����Һ�������ͣ�B����������������������������ΪҺ�壬������������Ϊ���壬�ҷ�Ӧ������ȣ����Է���װ��ѡB�������ռ�װ��ѡ��Ҫ����������ܶȼ�ˮ���ԡ�����ܶȱȿ�����ѡ�������ſ�������C��������ܶȱȿ���С��ѡ�������ſ�������E �������������ˮ��ѡ����ˮ����D�������⣬���ϻ������ſ������ռ�������ŵ㻹�У��ռ���������������ˮ���ռ�������ŵ��ǣ��ռ���������ϴ������ۺ�����������Ҫ��ȡ���ռ��ϴ�������������ѡBD��
��3���κι������ʣ������Ƿ�ĩ״�����ڱ���Ĺ����У���������һЩ�����е�ˮ�ݣ���Щˮ�ڼ��ȵ�ʱ��ͻ���ˮ�����ڽ�����Թܿ���ȴ�������Һ̬ˮ������ܿ����ϣ���Щˮ�ͻᵹ�����ȵĹܵף������Թܵ����ѡ�
��4�����ݣ�2���з���װ�õ�ѡ�����ݣ������Ƴ���Ӧ�ﶼӦ���ǹ��壬��ѡA��
���㣺���巢��װ�á��ռ�װ�õ�ѡ���ռ�װ�õıȽϣ���ȡ�����ı���ʽ��
27������������Ҫ�ɷ���FeO��TiO2�Ļ�����ȡ�����ѣ���ѧʽΪTi������Ҫ�����������£�

��1�����������е������������������ ����һ�ֻ�ѧʽ���ɣ������ڷǽ������ʵ��� ����һ�ֻ�ѧʽ���ɣ���TiO2����Ԫ�صĻ��ϼ��� ��
��2����������FeO��̼��Ӧ���ɶ�����̼��������Ӧ�ķ��ű���ʽ�� ��
��3���������п�ѭ�����õ������� ��
���𰸡�
��1��TiO2��FeO C ��Cl2 ��4
��2��FeO��C![]() Fe��CO2
Fe��CO2
��3��Mg
��������
���������
��1����������ָ����Ԫ����ɵĻ��������һ��Ϊ��Ԫ�ء����ݶ��壬��ΪTiO2��FeO��������ָͬһ��Ԫ����ɵĴ�����ǽ�����������ɵ��ʵ�Ԫ��Ϊ�ǽ���Ԫ�أ����ݶ��壬��ΪC ��Cl2���� �ݻ��������������ϼ۴�����Ϊ0��ԭ����ʽ�������Ԫ�صĻ��ϼۡ�
����Ԫ�صĻ��ϼ�X
X+��-2����2=0
���X=+4
��2����Ӧ������������ж���֪����Ӧ������ͼ�пɲ鵽������д����Ӧ�ı���ʽ��
��3��ѭ�����õ�������ָ�ڸ������У�����Ϊ��Ӧ����뵽�����У�����Ϊ��Ӧ������������������С������е�þ�ڵ�������Ӧ����Ϊ��Ӧ����֣������һ���Ȼ�þͨ��������Ϊ��������֣���þ��ѭ��ʹ�õ����ʡ�
���㣺���ʵ�ת��
28���˽̰��¿α껯ѧ�̲ľ��꼶�ϲ�
���ֽ���������������ķ�Ӧ�ж������̵Ĵ����������Լ���Ѱ���µĴ������о���ʵ�飬�����˻�ѧ̽��С�����Ȥ��
��������⡿�������ܷ�������������Һ�ֽ�Ĵ���������ܣ����Ч�����?
��ʵ��̽����
|
ʵ�鲽�� |
ʵ������ |
|
��.�ֱ���ȡ5mL5%����������Һ����A��B ��֧�Թ��У���A�Թ��м���ag��������Fe2O3����ĩ�����ֱ���A��B��֧�Թ��в��������ľ�����۲����� |
A�Թ��в������ݣ�������ľ����ȼ��B�Թ������������� |
|
���A�Թ���û��������ʱ�����¼������������Һ�����Ѵ����ǵ�ľ�������Թܣ���˷���������飬�۲����� |
�Թ��о��������ݣ�������ľ������ȼ |
|
��.��ʵ����е�ʣ������з��룬����������������ĩ����ϴ�ӡ�������������ù���������Ϊag�� |
|
|
���ֱ���ȡ5mL5%����������Һ����C��D ��֧�Թ��У���C�Թ��м���ag��������ĩ����D�Թ��м���ag�������̷�ĩ���۲����� |
|
��1���ڵ������У�Ҫʹʣ������������еIJ����� �������õ�������������̨�����������ձ��� ���������������� ��
 ��2���ڵ�����ʵ���У������õ�ΰ壨����ͼ��ʾ�������Թ�C��D��ɣ�
��2���ڵ�����ʵ���У������õ�ΰ壨����ͼ��ʾ�������Թ�C��D��ɣ�
�Ľ�����ŵ��� ��
��ʵ����ۡ�
��1��ʵ���������ֱ����֤������������ �� �ڷ�Ӧǰ���û�з����仯����������������ֽ�Ĵ�����
��2��д��ʵ������A�Թ��з�����Ӧ�ĵķ��ű���ʽ ��
��ʵ�����ۡ�
ʵ���������Ŀ���� ��
��ʵ�����۲쵽D�Թ��в������ݵ����ʸ��죬�ɴ�����Եõ��Ľ����� ��
��֪ʶ��չ��
(1)�������ϵ�֪��CuO��CuSO4�����Ρ���������Ҳ����������������Һ�ֽ�Ĵ����������йش�����˵������ȷ���� ��
A. ����ֻ�ӿ컯ѧ��Ӧ����
B.ͬһ����ѧ��Ӧ�����ж��ִ���
C. MnO2ֻ��������������Һ�ֽ�Ĵ���
D.�������������ʲ�������������Ӧ�ķ�Ӧ���������
(2) ���������ڷ��ú�ᷢѿ����ѿ�������к���һ���¶��ɷ��ѼC45H73O15N�����ֳ����������أ���һ�������Ե�߰������������߰������ʳ��δ�����ѿ���������������ж���
���Ѽ����Է�������Ϊ ��
���Ѽ����⡢������Ԫ�ص�Ԫ��������Ϊ ��
���Ѽ�����Ԫ�ص���������Ϊ ������������һλС������
��433.5g�Ѽ��к��� g̼Ԫ�ء�
���𰸡�
��ʵ��̽���������ˣ�©����������
����ԼҩƷ���������Ա����飨�𰸺������ɣ���
��ʵ����ۡ�����ѧ���ʺ�����
��H2O2![]() H2O��
O2
H2O��
O2
��ʵ�����ۡ���̽���������Ƿ�ȶ������̵Ĵ�Ч������
���������̵Ĵ�Ч������������
��֪ʶ��չ����B
�Ƣ�867 ��73:240 ��27.7% ��270
��������
���������
��ʵ��̽����
���ڵ������У�ʵ�ֵ��ǹ�����������Һ��ˮ�ķ��룬��ͨ������ʵ�֡������õ��������������⣬��ȱ��©����
���õ�ΰ�����Թܵ�����ŵ��ǽ�Լ��ҩƷ������
��ʵ����ۡ�
��ʵ������ʵ��Ŀ����Ϊ��˵���ù����������Ծ��иı�������ⷴӦ���ʵ���һ���ʣ�Ҳ����˵���Ļ�ѧ���ʱ��ֲ��䡣ʵ�����������ù���������Ϊag����������Ϊ��˵����Ӧǰ���������䡣
��ʵ������A�Թ��з����ķ�ӦΪ��������ķֽⷴӦ��������̲IJ�ͬ���Ǵ���������������������Ƕ������̡�
��ʵ�����ۡ�
��ʵ��������������Ϊ����֤��������⡿�е����������ܷ�������������Һ�ֽ�Ĵ�������һ���⣬��ʵ���������Ŀ��������Ϊ����֤��������⡿�е������Ч���������һ���⡣��ʵ����ƿ��Կ���������Ч���������ͨ����������������������бȽ�˵���ġ�
��ͨ����ʵ�����۲쵽D�Թ��в������ݵ����ʸ�������һ����������������̵Ĵ�Ч�����������á�
��֪ʶ��չ��
���������������ı�����ѧ��Ӧ�����ʣ������˵����Щ�����ܼӿ컯ѧ��Ӧ���ʣ���Щ���Ǽ�����ѧ��Ӧ�����ʡ���A����B.ͬһ����ѧ��Ӧ�����ж��ִ�������ȷ������˵��������ֽ⣬����������Ƕ������̣�Ҳ����������ͭ��Һ�����б������ᵽ���������ȡ����Դ�ѡB��C. MnO2ֻ��������������Һ�ֽ�Ĵ������������������ٻ�������طֽ�Ĵ�����D.�������������ʲ�������������Ӧ�ķ�Ӧ��������Ҳ�Ǵ���ģ�����������̣����Ǹ��������������������Ժ��ѧ������Ҳ��ʵ������ȡ�����ķ�Ӧ�
��2������Է������������ԭ������֮�͡��Ѽ����Է�������Ϊ12��45+1��73+16��15+14=867 ���Ѽ����⡢������Ԫ�ص�Ԫ��������Ϊ1��73��16��15=73��240 ���Ѽ�����Ԫ�ص���������Ϊ(16��15/867) ��100%=27.7% ��433.5g�Ѽ��к���̼Ԫ��Ϊ��(12��45/867) ��100%��433.5g=270g
���㣺���������ѧʽ���㣬���˲���

ͨѶ��ַ: ��������������Իƴ�����Է ��510660�����䣺lzm6308@163.com ��ϵQQ:534386438
Copyright © 2008-2012 klxkc.com All Rights Reserved. ��ICP��15026984��-1
