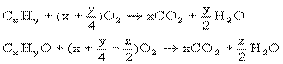| 上传:夏尊华化学 | 审核发布:admin | 更新时间:2015-6-7 19:12:15 | 点击次数:683次 |
|
课 题 |
有机物的研究步骤 |
课 型 |
新授 |
|
|
课 时 |
第2课时 |
主备课人 |
郭晟 |
|
|
复备课人 |
|
审核人 |
唐高明 |
|
|
课前准备 |
多媒体课件 |
|||
|
教 学 目 标 |
知识与技能: 1、了解测定有机化合物元素含量、相对分子质量的一般方法; 2、掌握确定有机化合物分子式的方法。 |
|||
|
过程与方法: 学会确定有机物的分子式。 |
||||
|
情感态度与价值观:通过联系知识与科学研究方法的关系,激发学生对化学学科的兴趣热爱。 |
||||
|
教学重点 |
有机化合物分子组成的确定 |
|||
|
教学难点 |
燃烧法的计算 |
|||
|
教学过程和教学内容 |
||||
|
二、元素分析与相对分子质量的测定 1、元素分析(燃烧法) 元素定量分析的原理是将一定量的有机物燃烧,分解为简单的无机物,并作定量测定,通过无机物的质量推算出组成该有机物元素原子的质量分数,然后计算出该有机物分子所含元素原子最简单的整数比,即确定其实验式。以便于进一步确定其分子式。 例1某含C、H、O三种元素的未知物A经燃烧分析实验测定该未知物碳的质量分数为52.16%,氢的质量分数为13.14%,试求(1)该未知物的实验式。 (2)若要确定它的分子式,还需要什么条件?
[练习]燃烧某有机物A 1.50g,生成1.12L(标准状况)
【总结】确定分子式的方法 2、相对分子质量的测定――质谱法 原理:
质荷比:
【巩固练习】 1.某烃0.1mol,在氧气中完全燃烧,生成13.2g CO2、7.2gH2O,则该烃的分子式为 。 2.125℃时,1L某气态烃在9L氧气中充分燃烧反应后的混合气体体积仍为10L(相同条件下),则该烃可能是 A. CH4 B. C2H4 C. C2H2 D.C6H6 3.室温下,一气态烃与过量氧气混合完全燃烧,恢复到室温,使燃烧产物通过浓硫酸,体积比反应前减少50mL,再通过NaOH溶液,体积又减少了40mL,原烃的分子式是 A. CH4 B. C2H4 C. C2H6 D.C3H8 4.使乙烷和丙烷的混合气体完全燃烧后,可得CO2 3.52 g,H2O 1.92 g,则该混合气体中乙烷和丙烷的物质的量之比为 A.1∶2 B.1∶1 C.2∶3 D.3∶4 5.两种气态烃的混合气共1mol,在空气中燃烧得到1.5molCO2和2molH2O。关于该混合气的说法合理的是 A.一定含甲烷,不含乙烷 B.一定含乙烷,不含甲烷 C.一定是甲烷和乙烯的混合物 D.一定含甲烷,但不含乙烯 6.25℃某气态烃与O2混合充入密闭容器中,点燃爆炸后又恢复至25℃,此时容器内压强为原来的一半,再经NaOH溶液处理,容器内几乎成为真空。该烃的分子式可能为 A. C2H4 B. C2H2 C. C3H6 D. C3H8 7.已知某烃A含碳85.7%,含氢14.3%,该烃对氮气的相对密度为2,求该烃的分子式。
|
||||
通讯地址: 广州市天河区东圃黄村龙怡苑 (510660)邮箱:lzm6308@163.com 联系QQ:534386438
Copyright © 2008-2012 klxkc.com All Rights Reserved. 粤ICP备15026984号-1