| 上传:郭晟化学 | 审核发布:admin | 更新时间:2017-12-20 23:32:00 | 点击次数:668次 |
第五章 物质结构 元素周期律
第三讲 化学键
【考纲解读】
|
考纲要求 |
真题统计 |
命题预测 |
|
1. 了解化学键的定义。 2.了解离子键、共价键的形成。 3.电子式、结构式的表示
|
2014・江苏卷,2 2015・全国卷Ⅱ,9 2015・海南卷,14
|
1. 化学键类型的判断与化合物类型的关系。这类知识的考查出现在选择题中,难度较小。 2. 8e-稳定结构、10e-或18e-粒子与电子式的书写。通常结合其他化学用语一起考查,如结构简式、结构式等。以选择题为主,有时推断题中的填空中也会出现,难度中等。 |
【自主复习检测】
1、说法是否正确,正确的画“√”,错误的画“×”。
(1)所有物质中都存在化学键。
(2)非金属元素的两个原子之间一定形成共价键,但多个原子间也可能形成离子键。
(3)(2012・高考天津卷3TB)不同元素的原子构成的分子只含极性共价键。
(4)金属元素和非金属元素间可能存在共价键
(5)(2012・高考大纲全国卷6TA)离子化合物中一定含有离子键。
【知识梳理】
1.化学键
使离子相结合或原子相结合的 通称为化学键。
一般化学物质主要由 或 结合而成。
2. 离子键和共价键
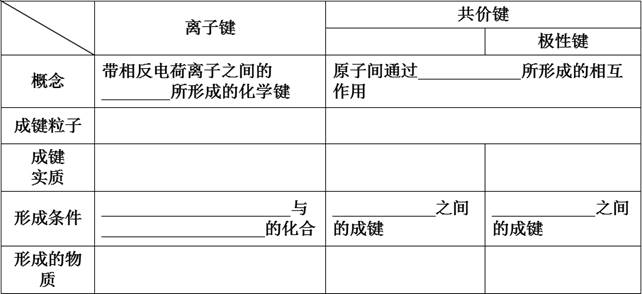 |
【思考感悟】
如何判断离子化合物与共价化合物?
【即时应用】
(1)(2010・高考海南卷)短周期元素X、Y、Z所在的周期数依次增大,它们的原子序数之和为20,且
Y2-与Z+核外电子层的结构相同。下列化合物中同时存在极性和非极性共价键的是( )
A.Z2Y B.X2Y2 C.Z2Y2 D.ZYX
(2)关于化学键的下列叙述中正确的是( )
A.离子化合物可能含共价键,共价化合物中可能含离子键
B.共价化合物可能含离子键,离子化合物中只 含离子键
C.构成单质分子的微粒一定含有化学键
D.在氧化钠中,除氧离子和钠离子的静电吸引作用外,还存在电子与电子、原子核与原子核之间的排斥作用
3.电子式的书写
(1)写出下列物质的电子式:
Ne S Mg
C2H2 NH3 N2
NH4Cl Na2O2 NaOH
【反思总结】
电子式的书写与正误判断电子式是表示微粒结构的一种式子,其写法是在元素符号的周围用“・”或“×”表示原子或离子的最外层电子,并用n+或n-(n为正整数)表示离子所带电荷。
(1) 原子的电子式:电子要尽可能的分布在元素符号的四
周。 如氮原子的电子式为_____,不能写成____或_____
(2) 离子的电子式:简单阳离子的电子式就是离子符号。如Mg2+既是镁离子符号,也是镁离子的电子式。复杂阳离子和阴离子,在标有“・”或“×”的离子符号外加方括号,方括号的右上角标明所带电荷。如:NH4+的电子式为_____,S2-的电子式为_____,Cl-的电子式为_____。
(3) 离子化合物的电子式:要注意每一个离子都与带相反电荷的离子直接相邻的事实。如:MgCl2的电子式为_____,不能写成_____ 或_____
(4) 共价型分子的电子式:要注意共用电子对的数目和表示方法。如:N2的电子式应为_____,不能写成_____ 或_____
(5) 要注意共价化合物与离子化合物的电子式的区别。前者不加括号,不写表示电荷的符号,后者阴离子和复杂的阳离子加方括号,括号外写表示电荷的符号。
【即时应用】
1.(1)(2016・全国Ⅱ卷)联氨(又称肼,N2H4,无色液体)分子的电子式为 ,其中氮的化合价为 。
(2)(2015・全国Ⅰ卷)以硼酸为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂,其电子式为 。
2.用电子式表示化合物的形成过程:
CaCl2 :
HCl :
【课堂总结】
一、离子键与共价键的比较
二、离子化合物与共价化合物的判断
三、电子式的书写
【巩固练习】
1.下列说法正确的是( )
A.CaH2晶体中的化学键是共价键
B.某物质在熔融态能导电,则该物质中一定含有离子键
C.含有阴离子的化合物一定是离子化合物
D.非金属原子间以共价键结合的物质都是共价化合物
2.(2015•海南卷,14)单质Z是一种常见的半导体材料,可由X通过如下图所示的路线制备。其中X为Z的氧化物;Y为氢化物,分子结构与甲烷相似。回答下列问题:
(1)能与X发生化学反应的酸是 ;由X制备Mg2Z的化学方程式为
(2) 由Mg2Z生成Y的化学方程式为 ,Y分子的电子式为
(3)Z、X中共价键的类型分别是 、
【课后思考】
1、化学键对物质性质的影响
2、从化学键的断裂与形成角度理解化学反应的本质
通讯地址: 广州市天河区东圃黄村龙怡苑 (510660)邮箱:lzm6308@163.com 联系QQ:534386438
Copyright © 2008-2012 klxkc.com All Rights Reserved. 粤ICP备15026984号-1

